A maggio 2026 un gruppo di ricercatori dell’Università della Pennsylvania ha presentato un sistema di intelligenza artificiale chiamato ApexGO, progettato per disegnare nuovi peptidi antibiotici partendo da molecole esistenti. Nei test di laboratorio, l’85% delle molecole generate dal sistema ha bloccato la crescita di batteri patogeni, e il 72% si è dimostrato più efficace dei composti originali. È uno dei segnali più concreti di come l’intelligenza artificiale stia cambiando il modo in cui si sviluppano nuovi farmaci.
La resistenza agli antibiotici, un problema urgente
Per capire l’importanza di ApexGO bisogna ricordare il contesto. Secondo l’Organizzazione Mondiale della Sanità, la resistenza antimicrobica è una delle dieci principali minacce sanitarie globali. Si stima che entro il 2050 le infezioni resistenti ai farmaci potrebbero causare circa 10 milioni di morti l’anno se non si interverrà. Da decenni l’industria farmaceutica fatica a immettere sul mercato nuovi antibiotici: i ritorni economici sono bassi rispetto ad altri ambiti terapeutici, e la chimica della scoperta tradizionale è lenta. L’intelligenza artificiale può accelerarne i passaggi più costosi.
Cosa fa ApexGO
ApexGO è un modello generativo di intelligenza artificiale addestrato su grandi database di peptidi – brevi catene di amminoacidi – dotati di attività antimicrobica. Riceve come input la sequenza di un peptide esistente e produce in uscita varianti modificate, progettate per migliorarne l’efficacia, ridurre la tossicità sulle cellule umane o aumentare la stabilità. Funziona in modo simile ad altri sistemi di IA generativa già famosi, ma applicato al linguaggio biochimico degli amminoacidi.
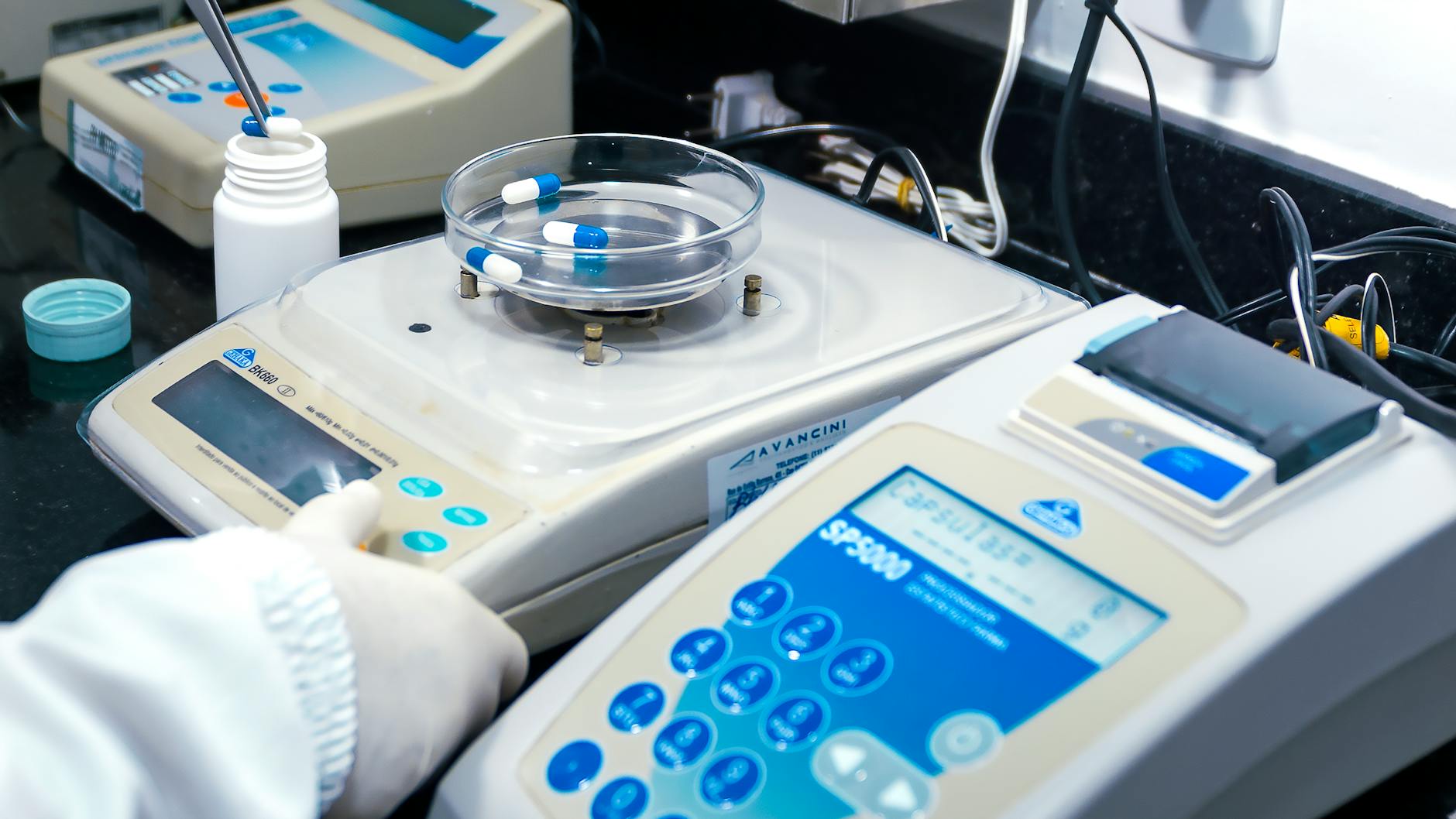
Come funziona in pratica
Il flusso di lavoro di un sistema come ApexGO segue tre fasi principali. Nella prima, l’IA genera in silico migliaia di possibili sequenze peptidiche, partendo da molecole note. Nella seconda fase, un secondo modello valuta ogni candidato predicendo proprietà come l’attività antibiotica, la solubilità e la potenziale tossicità. I migliori candidati vengono poi sintetizzati fisicamente in laboratorio e testati contro colture batteriche reali. È un imbuto che riduce drasticamente i tempi della scoperta classica, dove queste fasi richiedevano anni di lavoro umano.
Cosa sono i peptidi antimicrobici
I peptidi antimicrobici sono piccole molecole che molti organismi viventi, dagli insetti agli esseri umani, producono naturalmente per difendersi dalle infezioni. Sono parte del nostro sistema immunitario innato. Hanno attratto interesse farmaceutico perché agiscono spesso in modo diverso dagli antibiotici tradizionali, attaccando direttamente le membrane batteriche, e per questo i batteri sviluppano meno resistenza nei loro confronti. Il problema è che progettarli e ottimizzarli a tavolino è estremamente complesso: ci sono 20 amminoacidi possibili in ogni posizione, e una catena di 30 amminoacidi ha più combinazioni delle stelle nell’universo osservabile.
Perché serve l’intelligenza artificiale
Esplorare manualmente uno spazio di possibilità così vasto è impossibile per qualsiasi gruppo di ricerca umano. I modelli di IA, addestrati su milioni di esempi noti, possono apprendere quali combinazioni di amminoacidi hanno maggiore probabilità di essere efficaci e quali invece sono biologicamente inutili. Non si tratta di intuizione, ma di analisi statistica su grande scala: l’IA non sa «che cosa è» un antibiotico, ma riconosce le regolarità nei dati e propone nuove configurazioni plausibili.
Altri progetti nel settore
ApexGO non è isolato. Negli ultimi anni diversi gruppi di ricerca hanno annunciato risultati promettenti usando IA per la scoperta di farmaci. Nel 2020 i ricercatori del MIT pubblicarono su Cell la scoperta di halicina, un antibiotico identificato grazie al deep learning, in grado di colpire batteri resistenti alle terapie standard. Più di recente, la startup britannica DeepMind, sussidiaria di Alphabet, ha rivoluzionato la predizione della struttura tridimensionale delle proteine con il modello AlphaFold, valso il premio Nobel per la Chimica 2024 a Demis Hassabis e John Jumper.

I limiti da non dimenticare
L’intelligenza artificiale non è una bacchetta magica. Le molecole generate vanno sempre sintetizzate, testate in vitro e in vivo, e portate attraverso le fasi cliniche prima di poter essere usate sui pazienti. Tra la scoperta di una molecola promettente in laboratorio e la sua approvazione come farmaco passano in media dieci o quindici anni. L’IA accelera la prima parte, quella della scoperta, ma non azzera tempi e costi delle sperimentazioni cliniche, che restano la fase più lunga e costosa. Inoltre i modelli sono buoni quanto i dati su cui sono addestrati: bias e lacune nei database possono propagarsi nei risultati.
Le applicazioni oltre gli antibiotici
Lo stesso approccio sta venendo applicato a molti altri ambiti farmaceutici. Si stanno disegnando con IA generativa nuovi farmaci anticancro, terapie per malattie rare, vaccini personalizzati basati sull’mRNA, molecole per la lotta all’invecchiamento cellulare. Esistono start-up come Insilico Medicine, Generate Biomedicines, Exscientia e altre che hanno già portato candidati farmaci progettati da IA nelle fasi cliniche di sperimentazione. Per i pazienti, questo potrebbe tradursi in meno anni d’attesa per terapie efficaci contro malattie oggi incurabili.
L’aspetto regolatorio
Le agenzie regolatorie come la FDA statunitense e l’EMA europea stanno adattando le proprie procedure per valutare i farmaci scoperti tramite intelligenza artificiale. La questione cruciale è la spiegabilità: bisogna garantire che i ricercatori possano motivare scientificamente perché una determinata molecola dovrebbe funzionare, anche se la sua progettazione è stata mediata da un algoritmo. La regolamentazione resta una delle sfide più discusse, insieme alla proprietà intellettuale dei farmaci generati dall’IA.

Un cambio di paradigma
Vale la pena ricordare che molte delle scoperte annunciate con grande enfasi non si tradurranno necessariamente in farmaci commercializzati: la storia della farmacologia è piena di candidati promettenti che si sono fermati nelle fasi cliniche. Detto questo, la rapidità con cui sistemi come ApexGO producono molecole potenzialmente utili è qualitativamente nuova. Per chi si occupa di sanità pubblica, soprattutto in vista dell’emergenza della resistenza antimicrobica, è un segnale incoraggiante che merita attenzione.
Quando arriveranno in farmacia
Realisticamente, i primi antibiotici di nuova generazione progettati con IA potrebbero arrivare sul mercato non prima della fine degli anni Venti del Duemila. La trafila include trial preclinici sugli animali, tre fasi cliniche sull’uomo, valutazione regolatoria e produzione industriale. Per maggiori approfondimenti sulla resistenza antimicrobica si può consultare il portale dell’Organizzazione Mondiale della Sanità. Importante, in caso di sintomi sospetti, consultare sempre un medico e non interrompere mai gli antibiotici prima del tempo prescritto.
Se ti interessa il rapporto tra IA e medicina, leggi anche il nostro articolo sulla intelligenza artificiale in medicina.
Domande frequenti su ApexGO e IA per antibiotici
Cosa è ApexGO?
È un modello di intelligenza artificiale generativa sviluppato all’Università della Pennsylvania per progettare nuovi peptidi con attività antibiotica.
L’85% delle molecole generate è efficace, è un dato affidabile?
Si tratta di un dato di laboratorio, non clinico. Indica un’alta percentuale di candidati validi sui test in vitro contro colture batteriche, ma le fasi cliniche sono molto più selettive.
Si può comprare un antibiotico progettato da IA?
Non ancora. I farmaci attualmente in farmacia non sono progettati da IA. I primi candidati clinici basati su IA sono nelle fasi 1 e 2 di sperimentazione.
Cosa è la resistenza antimicrobica?
È la capacità dei batteri di sviluppare meccanismi che li rendono insensibili agli antibiotici. È una delle principali minacce sanitarie globali secondo l’OMS.
L’IA può sostituire i ricercatori farmaceutici?
No. L’IA è uno strumento che accelera alcune fasi del lavoro, ma la validazione sperimentale e clinica resta umana, così come la valutazione regolatoria e etica.
Come posso contribuire a contrastare la resistenza?
Usando gli antibiotici solo quando prescritti, completando sempre il ciclo terapeutico e mai conservando o riutilizzando antibiotici avanzati. Consulta sempre il medico in caso di dubbi.
